Glycerin
| Glycerol | |||
|---|---|---|---|
| |||
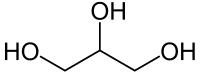 Glycerol | |||
| Danh pháp IUPAC | propan-1,2,3-triol | ||
| Tên khác | glycerin glycerine propantriol | ||
| Nhận dạng | |||
| Số CAS | 56-81-5 | ||
| PubChem | 753 | ||
| DrugBank | DB04077 | ||
| KEGG | D00028 | ||
| ChEBI | 17522 | ||
| ChEMBL | 692 | ||
| Mã ATC | A06AG04,A06AX01 (WHO) , QA16QA03 | ||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| UNII | PDC6A3C0OX | ||
| Thuộc tính | |||
| Bề ngoài | chất lỏng không màu hygroscopic | ||
| Mùi | không mùi | ||
| Khối lượng riêng | 1,261 g/cm³ | ||
| Điểm nóng chảy | 17,8 °C (290,9 K; 64,0 °F) | ||
| Điểm sôi | 290 °C (563 K; 554 °F) | ||
| Chiết suất (nD) | 1,4746 | ||
| Độ nhớt | 1,412 Pa·s[1] | ||
| Các nguy hiểm | |||
| MSDS | JT Baker | ||
| NFPA 704 |
1 1 0 | ||
| Điểm bắt lửa | 160 °C (320 °F) (cốc kín) 176 °C (349 °F) (cốc hở) | ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa).  Y kiểm chứng (cái gì Y kiểm chứng (cái gì  Y Y N ?) N ?)Tham khảo hộp thông tin | |||
Glycerol hay glyxerol, glycerin, glyxerin là một alcohol đa chức, gồm 3 nhóm -OH gắn vào gốc hydrocarbon C3H5 (công thức hóa học là C3H5(OH)3 hay C3H8O3).
Glycerol là một thành phần quan trọng tạo nên chất béo, thuốc nổ nitroglycerin...
Nó có một số tính chất của một polyol như phản ứng với Cu(OH)2 tạo ra dung dịch xanh trong suốt. Đây cũng là phản ứng đặc trưng để nhận biết alcohol đa chức có 2 nhóm -OH trở lên gắn liền kề nhau. Lipid có thể chuyển hóa thành glycerin thông qua dịch mật và enzym lipase.
Tính chất hóa học
Phản ứng với kim loại kiềm
Như các alcohol khác, glycerol phản ứng với kim loại kiềm, tạo thành glycerat tương ứng và giải phóng hydro:
Phản ứng với đồng(II) hydroxide
Glycerol hòa tan được đồng(II) hydroxide, tạo thành phức đồng(II) glycerat ở dạng màu xanh lam trong suốt.
Phản ứng cháy
Oxy hóa hoàn toàn glycerol bằng cách đốt cháy với oxy, thu được anhydride carbonic và nước:
Phản ứng với acid nitric
Thông thường, glycerol khi phản ứng với acid nitric sẽ bị thế các nhóm hydroxy, tạo thành nitroglycerin (glyceryl trinitrat):
Tuy nhiên nó cũng có thể bị oxy hóa bởi acid nitric (hoặc một số tác nhân khác) tạo thành acid glyceric (acid α,β-dihydroxypropionic):[2]
Điều chế
Glycerol là sản phẩm phụ của quá trình xà phòng hóa các triglyceride:
Tham khảo
- ^ “Viscosity of Glycerol and its Aqueous Solutions”. Truy cập ngày 19 tháng 4 năm 2011.
- ^ Ngô, Thị Thuận; Đặng, Như Tại (2023). “Chương 12: Axit cacboxylic. Dẫn xuất của axit cacboxylic. Dẫn xuất của axit cacbonic. Axit sunfonic và dẫn xuất”. Hóa học Hữu cơ - tập hai. Nhà xuất bản Giáo dục Việt Nam. tr. 149. ISBN 978-604-0-37519-3.
 | Bài viết liên quan đến hóa học này vẫn còn sơ khai. Bạn có thể giúp Wikipedia mở rộng nội dung để bài được hoàn chỉnh hơn.
|




![{\displaystyle {\ce {2C3H8O3 + Cu(OH)2 -> [C3H5(OH)2O]2Cu + 2H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/68b24d9054e690bc75f11df443652a39af02387d)
![{\displaystyle {\ce {2C3H8O3 + 7O2 ->[{t°}] 6CO2 + 8H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/897bfaf8d9686c1cc13299763ea338b4c3abe093)


![{\displaystyle {\ce {C3H5(OOCR)3 ->[{NaOH}][{t°}] C3H5(OH)3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f7683d59721a2c9d9341c5cebff773e022746fdf)










